Влияние противовирусной терапии на частоту развития бактериальных осложнений и назначения антибактериальных препаратов для системного использования у пациентов с ОРВИ и гриппом (результаты международного когортного наблюдательного исследования FLU-EE)
2 Ярославский государственный медицинский университет Минздрава России, Ярославль
3 Московский государственный медико-стоматологический университет им. А.И. Евдокимова, Москва
4 Первый московский государственный медицинский университет им. И.М. Сеченова, Москва
5 Ереванский государственный медицинский университет им. Мхитара Гераци, Ереван, Армения
6 Институт медицинской биотехнологии им. Вл. Бахуташвили Тбилисского Государственного медицинского университета, Тбилиси, Грузия
7 Государственный университет медицины и фармации им. Николае Тестемицану, Кишинев, Республика Молдова
2 Yaroslav State Medical University, Department of Infection Diseases, Epidemiology and Pediatric Infections
3 Moscow State Medical and Stomatological University by A.I.Evdokimov , Department of Infection Diseases
4 First Moscow State Medical University by I.M.Sechenov , Department of Human Pathology
5 Erevan State Medical University by Mhitar Geraci, Department of Internal Diseases Diagnostics
6 Institute of Medical Biotechnology by V.Bahutashvili, Tbilissi State Medical University, Department of Immunoreabilitation
7 State University of Medicine and Pharmacy by N.Testemicianu, Department of Internal Diseases, Reumatology and Nephrology, Moldova
Цель. Оценка частоты развития бактериальных осложнений и антибиотикотерапии у амбулаторных пациентов с ОРВИ и гриппом с анализом эффективности противовирусного лечения. Материал и методы. Проведено международное когортное открытое неинтервенционное исследование «Лечение ОРВИ и гриппа в рутинной клинической практике». Проанализированы результаты лечения 18946 пациентов в возрасте 18-93 лет с установленным клинически диагнозом ОРВИ или гриппа, проходивших амбулаторное лечение в 262 центрах России, Молдовы, Армении и Грузии. Одна группа пациентов получала лечение согласно принятым и применяемым в соответствующей стране схемам комплексного лечения ОРВИ и гриппа; в другую группу вошли пациенты, получавшие в составе комплексного лечения противовирусный препарат Кагоцел® (Россия). На каждом из трёх визитов оценивали клиническую симптоматику (в баллах), наличие бактериальных осложнений, эффективность назначенной лекарственной, в т.ч. антибактериальной, терапии. Результаты. Бактериальные осложнения зарегистрированы в 8,3% случаев, а системные антибиотики назначались врачами в 9,3%. Частота развития бактериальных осложнений и назначения системных антибиотиков увеличивается пропорционально возрасту пациентов, тяжести заболевания, срокам обращения к врачу и начала лечения. Назначение препарата кагоцел в составе комплексного лечения гриппа и ОРВИ способствует сокращению числа бактериальных осложнений в 1,65 раза (р<0,01), а также снижению назначения системной антибактериальной терапии в 1,51 раза (р<0,01), что приводит к улучшению исхода заболевания при различных сроках начала терапии. Максимальная эффективность и меньшее число осложнений лечения зарегистрировано у лиц трудоспособного возраста. Выводы. Противовирусная терапия показала свою эффективность при лечении ОРВИ и гриппа, ее применение приводит к снижению частоты развития бактериальных осложнений.
Ключевые слова: острая респираторная вирусная инфекция, грипп, бактериальные осложнения, противовирусная терапия, кагоцел, антибактериальная терапия.
Objective: to evaluate the incidence of bacterial aggravations and antibiotics administration with analysis of effectiveness of antiviral therapy in ambulatory patients with acute viral respiratory infection (ARVI) and influenza. Material and methods. International cohort open non-interventional study «Treatment of ARVI and influenza in routine clinical practice» was conducted. The data analysis covers treatment results of 18946 ambulatory patients aged 18–93 years with clinical diagnosis of ARVI or influenza in 262 centers in Russia, Moldova, Armenia and Georgia. One group of patients received treatment in accordance with approved and applicable in their country schemes of complex treatment of ARVI and influenza; other group included patients treated with the complex treatment including antiviral drug Kagocel® (Russia). On each of 3 visits were evaluated clinical symptoms (in scores), the presence of bacterial aggravations, and the effectiveness of drug treatment including antibacterial therapy. Results. Bacterial aggravations were recorded in 8.3% cases, and systemic antibiotics were prescribed by doctors in 9.3% cases. The incidence of bacterial aggravations and administration of systemic antibiotics increased proportionally to the age of patients, severity of disease, times of first visit to the doctor and the start of treatment. Prescription of Kagocel® in the complex treatment of ARVI and influenza contributes to reduction of number of bacterial aggravations in 1.65 times (p<0.01) and decreases necessity of systemic antibiotic therapy in 1.51 times (p<0.01), which leads to better disease outcome at various therapy start times. Maximum efficiency and fewer treatment aggravations were recorded for working age patients. Conclusions. Antiviral therapy has shown its effectiveness in the treatment of ARVI and influenza, its implementation leads to decrease of bacterial aggravations incidence.
Key words: influenza, acute respiratory viral infection, bacterial complications, antiviral therapy, Kagocel®, antibacterial therapy.
Введение
Острые респираторные вирусные инфекции (ОРВИ) и грипп остаются в центре внимания клинической медицины, что связано с регулярно повторяющимися эпидемиями и значительными трудопотерями. Во время тяжёлых эпидемий, вызываемых вирусом гриппа, в эпидемический процесс вовлекаются до 50% населения 1, 2, 3. В России регистрируется 27,3—41,2 млн случаев ОРВИ в год, доля которых достигает 95% в структуре всех инфекционных заболеваний 1, 4.
Интоксикация, а также другие последствия ОРВИ и гриппа могут стать причиной обострения уже имеющихся соматических (в т.ч. хронических) заболеваний и присоединения различных бактериальных инфекций, а в тяжелых случаях и смерти больных. От ОРВИ и гриппа ежегодно в мире умирают около 4,5 млн человек, при этом на долю вируса гриппа приходится около 250 тыс летальных исходов 3, 4. В России при заболевании гриппом наиболее высокая частота госпитализаций отмечается в возрастной группе от 18 до 64 лет, а летальность в отделениях реанимации достигает 46%. Основными причинами летального исхода являются тяжелое течение, сопровождающееся развитием одно- или двусторонних вирусных пневмоний, регистрирующихся у 30% взрослых госпитализированных пациентов, а также развитие бактериальных осложнений и полиорганной недостаточности 5. Частота бактериальных осложнений составляет по данным разных авторов от 7,5 до 23% 6, 7, 8.
Антибактериальная терапия для системного применения необходима в случае развития бактериальных осложнений. Также она рекомендуется с профилактической целью при тяжелых формах ОРВИ и гриппа пациентам с синуситами, ринитами, отитами и другими хроническими патологиями. При легком и среднетяжелом течении ОРВИ назначение антибиотиков не рекомендуется 9, 10, так как это может вызвать развитие лекарственной устойчивости возбудителей, а также замедлить процесс выздоровления и ухудшить исход в связи с побочными и нежелательными явлениями антибиотикотерапии. Вопросы применения системных антибиотиков при ОРВИ и гриппе до сих пор остаются дискутабельными. Ряд авторов полагают, что роль бактериальной инфекции сильно переоценена, а назначение антибактериальной терапии происходит значительно чаще, чем требуется 11, 12.
Учитывая эпидемиологическую актуальность, ВОЗ рекомендует вакцинацию населения от гриппа. Однако постоянные изменения штаммов вирусов не позволяют заранее точно предсказать будущую угрозу. Это ставит под сомнение вакцинацию в качестве единственного патогенетически обоснованного метода профилактики гриппа. Поэтому поиск эффективных универсальных противовирусных препаратов остается по-прежнему актуальной задачей.
Для изучения эффективности существующих схем лечения ОРВИ и гриппа было проведено когортное многоцентровое международное открытое неинтервенционное исследование FLU-EE «Лечение ОРВИ и гриппа в рутинной клинической практике» 13. Целью настоящей работы является оценка частоты развития бактериальных осложнений и частоты назначения системных антибактериальных препаратов у пациентов с ОРВИ и гриппом с анализом эффективности противовирусного препарата кагоцел. Основными задачами данной работы стали: изучение назначаемых при гриппе и ОРВИ лекарственных средств; анализ частоты осложнений ОРВИ и гриппа, требующих назначения системных антибиотиков (АБ), а также частоты назначения АБ, в т.ч. в зависимости от возраста пациентов и сроков начала лечения; изучение влияния препарата кагоцел на частоту развития бактериальных осложнений и частоту назначения системных АБ с анализом групп АБ по международной классификации (коды АТХ); изучение исхода заболевания и сроков выздоровления в группах пациентов, получавших и не получавших препарат кагоцел.
Материалы и методы
Проанализированы результаты лечения 18 946 пациентов, в том числе 8 085 мужчин (42,7%) и 10 861 женщин (57,3%), в возрасте от 18 до 93 лет (средний возраст 42,7±15,1 лет, медиана 40 лет) с клинически установленным диагнозом гриппа или ОРВИ, проходивших амбулаторное лечение в 262 лечебно-профилактических учреждениях России, Молдовы, Армении и Грузии. 79,6% (n=15 087) человек были трудоспособного возраста (согласно ТК РФ: женщины до 55 лет, мужчины до 60 лет), 20,4% (n=3 859) пациентов были пенсионного возраста. Обращение за медицинской помощью на 1—2 сутки заболевания (раннее) было зарегистрировано в 76,8% (n=14 555) случаях, включая 7 437 (39,3%) пациентов, обратившихся и начавших получать соответствующее лечение с 1-х суток заболевания. На 3 день и позднее с момента появления первых симптомов гриппа и ОРВИ к врачу обратилось 4 391 (23,2%) человек, которые были отнесены к подгруппе позднего обращения.
По окончании исследования для анализа результатов пациенты были разделены на группы в зависимости от назначенной противовирусной терапии. Одна группа была сформирована из пациентов, которые получали комплексное лечение ОРВИ и гриппа по схемам, применяемым в этих странах (группа сравнения, n=1 680), другая группа дополнительно в составе комплексного лечения получала противовирусный препарат кагоцел (n=17 266). Пациенты обеих групп были сопоставимы по полу, возрасту, тяжести заболевания и срокам обращения за медицинской помощью.
Согласно протоколу исследования, анализировались данные 3 визитов пациента к врачу без регламентирования промежутков времени между ними. В среднем 2-й визит проводился через 3 суток (при межквартильном интервале 3 / 4 день), 3-й визит — через 6 дней после первого (при межквартильном интервале 5 / 8 день). На каждом визите осуществлялась оценка состояния пациентов с регистрацией выраженности клинических симптомов (температура тела, озноб, слабость, боль в мышцах и/или суставах, ринит, зуд в горле, кашель, склерит/ конъюнктивит, головная боль), проводилось измерение артериального давления и числа сердечных сокращений. Выполнялась оценка назначенной в динамике лекарственной терапии, а также оценка осложнений, требующих назначения системных антибиотиков.
Этические вопросы. Проведение исследования «Лечение ОРВИ и гриппа в рутинной клинической практике» на территории РФ было одобрено Независимым междисциплинарным Комитетом по этической экспертизе клинических исследований. Оно получило одобрение Локального этического комитета Федерального государственного бюджетного учреждения высшего образования «Казанский государственный медицинский университет». Проведение исследования FLU-EE в Армении, Грузии и на территории Молдовы было одобрено «Фрайбургским международным Этическим Комитетом», на территории Армении исследование получило так же одобрение Комитета по Этике Ереванского государственного медицинского университета им. Мхитара Гераци. В Грузии исследование было одобрено «Национальным центром контроля заболеваний и общественного здоровья».
Статистическая обработка результатов исследования проведена с использованием программы SPSS с применением стандартных параметрических и непараметрических критериев оценки статистической значимости. Различия считались достоверными при p<0,05. Описательная статистика качественных параметров представлена в виде частот (абс, %), количественных — медиана (Ме), средне ± стандартное отклонение, а также нижний и верхний квартиль в случае, когда параметр имел функцию распределения, далекую от нормального. Нормальным принималось распределение, у которого критерий отличия Колмогорова-Смирнова от теоретически нормального распределения был выше 0,05. Для сравнения двух независимых непараметрических выборок использовали критерий Манна-Уитни, для множественного сравнения — Краскелла-Уоллиса. Для сравнения двух зависимых непараметрических выборок использовали критерий Уилкоксона, для множественного сравнения — Фридмана. Количественные данные с нормальным распределением оценивали с помощью теста Стьюдента, а также Ньюмана-Кейлса для множественных сравнений. Качественные переменные сравнивались с помощью теста χ2 (хи-квадрат Пирсона, анализ таблиц сопряженности).
Результаты
При анализе назначенной терапии было установлено, что число назначаемых препаратов варьировало от 1 до 11, в среднем (медиана) пациенты получали 3 препарата на протяжении всего исследования. Согласно международной классификации лекарственных средств по кодам АТХ, наиболее часто назначались препараты группы J (противомикробные средства для системного применения), их получали 17 680 человек (93,3%), а также препараты группы R (для лечения патологий дыхательной системы), которые были назначены 11 137 (58,8%) пациентам (табл. 1). На третьем месте по частоте назначались препараты группы N (нервная система; n=4 783; 25,2%) за счет входящих в эту группу жаропонижающих средств (анилинов), на четвертом — препараты группы М (костно-мышечная система; n=2 663; 14,1%) преимущественно за счет входящих в эту группу НПВС, назначаемых с той же целью; на пятом — препараты группы А (пищеварительный тракт и обмен веществ; n=2085; 11,0%) за счет входящих в эту группу средств, предназначенных для лечения заболеваний полости рта и витаминов. Для лечения гриппа и ОРВИ использовали различные средства за исключением препаратов групп В, С, D, G, H, при этом число одновременно получаемых препаратов для ОРВИ и гриппа варьировало от 1 до 8 (Ме=3).
| Группа лекарственных средств | Абс. (n) | % | |
|---|---|---|---|
| A | Пищеварительный тракт и обмен веществ | 2085 | 11,0 |
| B | Препараты, влияющие на кроветворение и кровь | 444 | 2,3 |
| C | Сердечно-сосудистая система | 1643 | 8,7 |
| D | Лечение заболеваний кожи (дерматология) | 351 | 1,9 |
| G | Мочеполовая система и половые гормоны | 20 | 0,1 |
| H | Гормональные препараты | 47 | 0,2 |
| J | Противомикробные для системного использования | 17680 | 93,3 |
| L | Противоопухолевые и иммунные препараты | 217 | 1,2 |
| M | Костно-мышечная система | 2663 | 14,1 |
| N | Нервная система | 4783 | 25,2 |
| R | Дыхательная система | 11137 | 58,8 |
| S | Органы чувств | 170 | 0,9 |
| V | Прочие препараты | 51 | 0,3 |
Системные антибиотики (АБ) были назначены 1 764 (9,3%) пациентам. Однако осложнения, требующие назначения АБ, были зарегистрированы у 1 580 (8,3%) пациентов. В числе осложнений в основном врачи чаще регистрировали бронхит и трахеобронхит, реже синусит, отит, ангину, пневмония была диагностирована лишь в 0,7% случаев, при этом большинство бактериальных осложнений течения ОРВИ и гриппа регистрировались на 2-м визите. АБ с профилактической целью (без диагностированного бактериального осложнения) были назначены 299 (1,6%) пациентам. В 115 (0,6%) случаях были зарегистрированы осложнения, требующие назначения АБ, однако пациентам их не назначили, в основном по причине добровольного отказа от антибиотикотерапии.
Наиболее часто врачи назначали препараты групп J01С (пенициллины, n=740/1 764; 42,0%) и J01F (макролиды, линкозамиды; n=686/1 764; 38,9%). Другие АБ для системного применения (тетрациклины — J01А, другие бета-лактамы — J01D, сульфаниламиды — J01E, производных хинолона — J01M, прочие АБ — J01X) назначались 341 пациенту (19,3%).
Среди препаратов пенициллинового ряда чаще был назначен амоксициллин (n=467/1 764; 25,9%), бета-лактамные пенициллины в сочетании с клавулановой кислотой назначали в 1,63 раза реже (n=281/1 764; 15,9%). Ампициллин был назначен лишь одному пациенту, при этом на 3 визите его сменили на амоксициллин. Сультамициллин получали 4 человека (0,2%).
Группу других бета-лактамов (J01D) применяли в 4,77 раза реже, чем АБ пенициллинового ряда (n=155/1 764; 8,8%). Среди других системных бета-лактамных антибиотиков чаще был назначен цефтриаксон (n=73/1 764; 4,1%) и цефиксим (n=68/1 764; 3,9%). Другие цефалоспорины применяли гораздо реже.
Группа J01F в основном представлена макролидами, среди которых лидирующую позицию занимал азитромицин (n=487/1 764; 27,6%) и кларитромицин (n=169/1 764; 9,6%). Значительно реже назначали джозамицин (n=21/1 764; 1,2%), спирамицин (n=3/1 764; 0,2%) и эритромицин (n=2/1 764; 0,1%). Линкозамиды (линкомицин) использовали в единственном случае.
Группа производных хинолона (J01М) применялась у 169 пациентов. Преимущественно она представлена фторхинолонами, из которых чаще назначали ципрофлоксацин (n=86/1 764; 4,9%) и левофлоксацин (n=75/1 764; 4,3%). Гемифлоксацин был назначен 3 пациентам (0,2%), другие представители группы J01М (офлоксацин, норфлоксацин, моксифлоксацин) использовались крайне редко (n=1/1 764; 0,1%).
Тетрациклины (J01A) были назначены всего 2 пациентам (0,11%), сульфаниламиды (J01E) – 8 (0,45%).
Прочие АБ для системного использования (группа J01Х) были назначены 7 пациентам (0,4%), в том числе метронидазол (n=1/1 764; 0,1%), нитроксолин (n=1/1764; 0,1%) и гидроксиметилхиноксалиндиоксид (n=5/1764; 0,3%).
Предварительное микробиологическое исследование на определение чувствительности для подбора оптимальной антибиотикотерапии в большинстве случаев не проводилось, что в условиях амбулаторной практики часто наблюдается.
Частота развития бактериальных осложнений и частота назначения антибиотиков для системного использования при ОРВИ и гриппе увеличивалась пропорционально возрасту пациентов, тяжести заболевания, а также срокам начала лечения (рис. 1). Отсроченное начало лечения ОРВИ и гриппа (с 3 суток и позднее) по сравнению с ранним (на 1—2 сутки заболевания) сопровождалось значимым ростом числа осложнений в 2,48 раза (с 6,2 до 15,4%) и частоты антибиотикотерапии в 2,41 раза (с 7,0 до 16,9%).
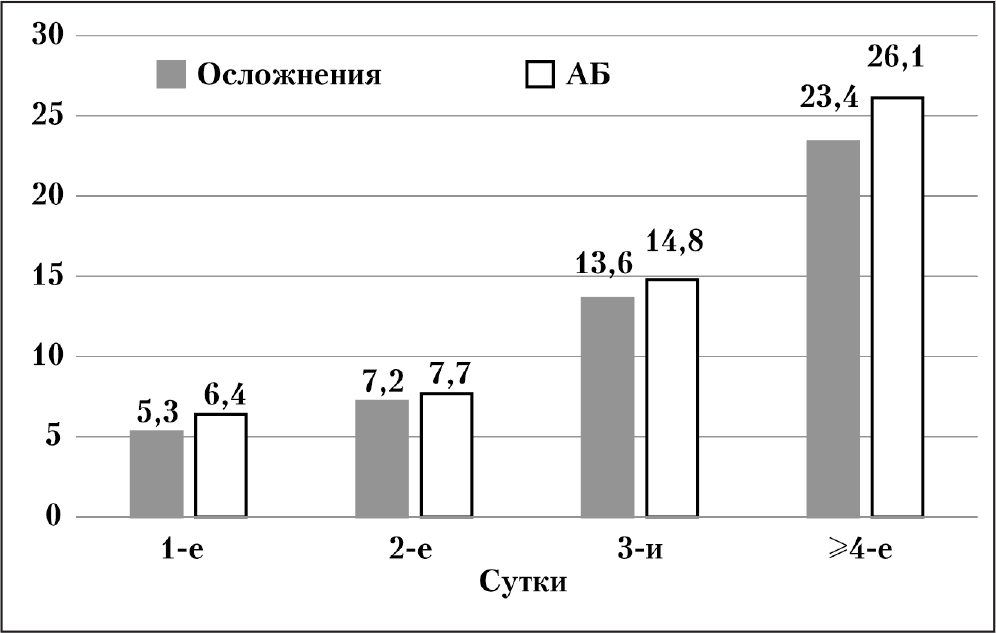
Среди пациентов, у которых на первом визите была установлена легкая степень тяжести, частота назначения системных антибиотиков составила 2,7%, средняя — 8,7%, тяжелая — 13,5% (р<0,001). Увеличение частоты назначения системных АБ пропорционально возрасту (от 8,2% в трудоспособном до 13,7% в пенсионном) и, вероятно, может быть связано с сопутствующей хронической соматический патологией, сопровождающейся иммунными нарушениями. Наименьшее число осложнений гриппа и ОРВИ, требующих назначения АБ (менее 10%) зарегистрировано при начале лечения в первые три дня от момента появления клинических симптомов у пациентов в возрасте до 50 лет. Максимальное число осложнений, сопряженных с назначением системных АБ зарегистрировано при позднем начале лечения у пациентов старших возрастных групп.
В ходе исследования было установлено, что назначение противовирусного препарата кагоцел способствует сокращению числа пациентов с бактериальными осложнениями гриппа и ОРВИ и частоты назначения системных антибактериальных препаратов. Так, осложнения, требующие назначения антибиотиков были зарегистрированы у 8,3% (n=1 580) пациентов, в том числе у 7,9% пациентов из группы кагоцел (n=1 361) и 13,0% группы сравнения (n=219). Межгрупповое различие в 1,65 раза является значимым (p<0,001). Системные антибиотики были назначены в 8,9% (n=1 539) случаев в группе препарата кагоцел и в 13,4% (n=225) случаев в группе сравнения, что в 1,51 раза больше (p<0,001).
Анализ частоты назначения системных АБ в зависимости от сроков начала лечения ОРВИ и гриппа показал (рис. 2), что при ранней терапии (1—2 сутки от дебюта заболевания) в группе пациентов, получавших кагоцел, частота назначения системных антибиотиков составила 6,6% (873/13 237), в то время как при отсутствии противовирусной терапии системные антибиотики были назначены 11,4% (150/1 318) пациентам, что статистически значимо в 1,73 раза больше (p<0,001). Наиболее существенная разница между группами выявлена среди пациентов, обратившихся за медицинской помощью на 1-е сутки заболевания (5,9% в группе кагоцела и 11,7% в группе сравнения; р<0,001). При позднем начале лечения (на 3—7 сутки) в группе кагоцела частота назначения увеличилась до 16,5% (666/4 029). Однако в группе сравнения системные антибиотики были применены у 20,7% (75/362) пациентов, т.е. в 1,26 раза чаще (p=0,027).
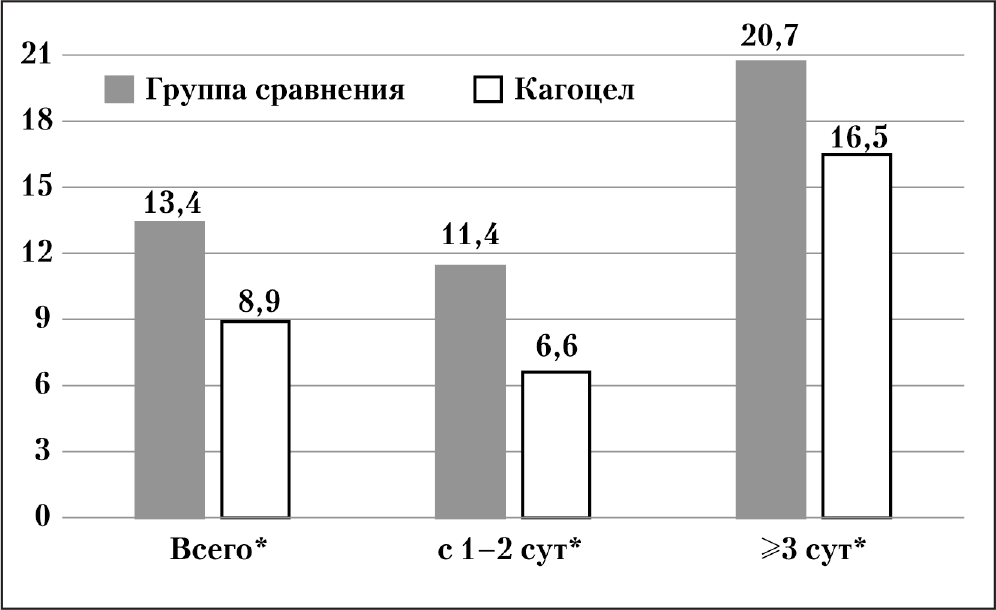
Аналогичные позитивные результаты обнаружены при анализе частоты бактериальных осложнений в зависимости от сроков начала лечения (табл. 2). Среди пациентов, обратившихся к врачу на 1-е сутки заболевания, требующие назначения АБ осложнения были зарегистрированы в 4,7% случаях в группе кагоцела и в 11,2% случаев в группе сравнения, что в 2,38 раза больше (р<0,001). Назначение препарата кагоцел приводило также к сокращению числа осложнений среди пациентов, обратившихся к врачу на 2-е сутки заболевания, в 1,63 раза (р<0,001), а начавших лечение с 3—7 суток — в 1,33 раза (р=0,009).
| Группа сравнения | Кагоцел | p | Итого | ||
|---|---|---|---|---|---|
| 1-е сут | Осложнения | 77 (11,2%) | 317 (4,7%) | <0,001 х2=52,88 | 394 (5,3%) |
| Без осложнений | 609 (88,8%) | 6433 (95,3%) | 7042 (94,7%) | ||
| 2-е сут | Осложнения | 70 (11,1%) | 439 (6,8%) | <0,001 х2=16,2 | 509 (7,2%) |
| Без осложнений | 561 (88,9%) | 6047 (93,2%) | 6608 (92,8%) | ||
| ≥3-и сут | Осложнения | 72 (20,0%) | 605 (15,0%) | 0,009 х2=6,29 | 677 (15,4%) |
| Без осложнений | 288 (80,0%) | 3424 (85,0%) | 3712 (84,6%) | ||
Анализ частоты бактериальных осложнений и назначения системных АБ в разных возрастных группах пациентов, показал, что кагоцел эффективен в любом возрасте (рис. 3). Осложнения, требующие назначения АБ, реже были зарегистрированы у пациентов трудоспособного возраста — 6,9% (962/13862) в группе кагоцела и у 11,9% пациентов (146/1222) группы сравнения, что в 1,72 раза чаще (p<0,001). У женщин старше 55 лет и мужчин старше 60 лет осложнения были в 11,7% (399/3403) и 16,0% (73/455) случаях соответственно (p=0,006). АБ пациентам трудоспособного возраста были назначены в 7,8% (1087/13862) случаях в группе пациентов, получавших кагоцел, а в группе сравнения — 12,0% (147/1222), что в 1,54 раза больше (p<0,001). Пациенты пенсионного возраста АБ получали чаще — 13,3% (452/3403) в группе кагоцела и 17,1% (78/455) в группе сравнения, что в 1,29 раза больше (p=0,017).
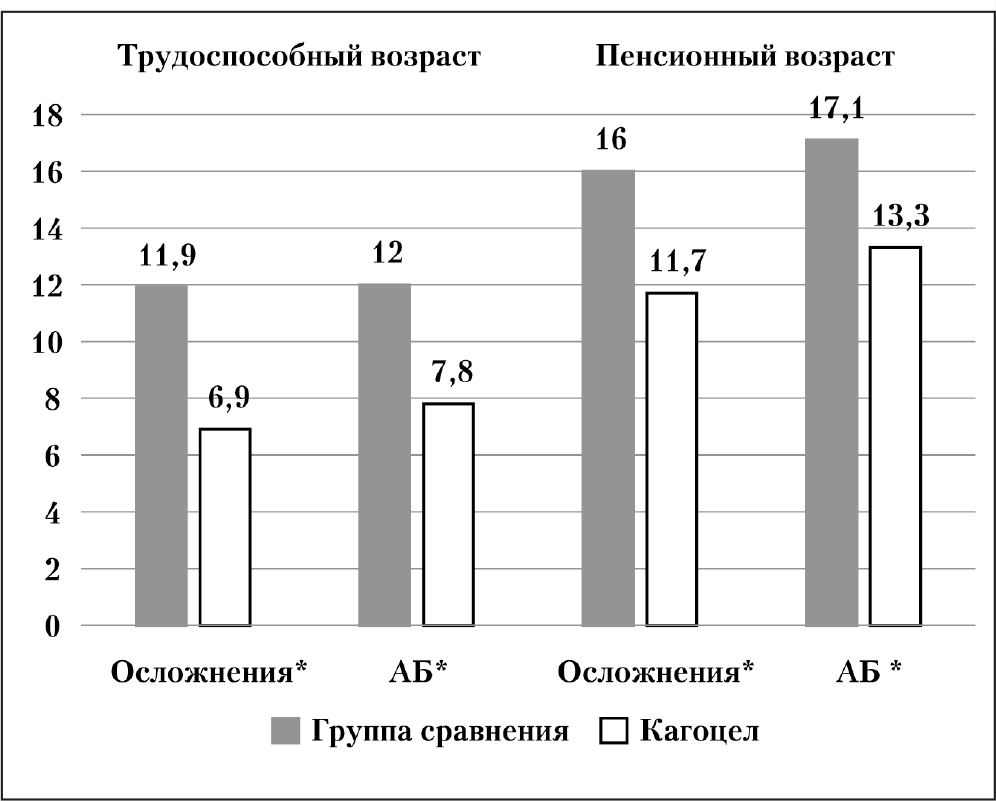
Назначение препарата кагоцел привело к сокращению применения всех групп системных АБ (p<0,001), особенно пенициллинов и непенициллиновых бета-лактамов (см. табл. 3). Так, пенициллины получали 3,7% (637/17 266) пациентов из группы кагоцела и 6,1% (103/1 680) пациентов группы сравнения, что достоверно в 1,65 раза чаще. В большей степени при назначении кагоцела отмечено снижение назначения амоксициллина (в 2,18 раза с 4,8 до 2,2%; p<0,01). Частота назначения бета-лактамных пенициллинов в обеих группах была сопоставимой, но другие бета-лактамные АБ получали 0,7% (119/17 266) пациентов из группы кагоцела и 2,1% (36/1 680) пациентов группы сравнения, что достоверно в 3 раза больше. В частности, при назначении кагоцела установлено уменьшение применения цефтриаксона в 4 раза с 1,2 до 0,3% (p<0,05). Зарегистрирована также тенденция к сокращению частоты назначения макролидов в 1,08 раза.
| Группа | МНН | код ATX | Всего назначено антибиотиков (n=1764) |
Группа сравнения (n=1680) |
Кагоцел (n=17266) |
|---|---|---|---|---|---|
| Тетрациклины | Доксициклин | J01AA02 | 2 | 0 (0,00%) | 2 (0,01%) |
| Пенициллины, в т.ч. бета-лактамные |
Амоксициллин | J01CA04 | 454 | 81 (4,8%) | 373 (2,2%) |
| Амоксициллин+ Клавулановая кислота | J01CR02 | 279 | 21 (1,3%) | 258 (1,5%) | |
| Ампициллин, Амоксициллин |
J01CA01, J01CA04 |
1 | 0 (0,00%) | 1 (0,01%) | |
| Амоксициллин, Амоксициллин+ Клавулановая кислота |
J01CA04, J01CR02 |
2 | 1 (0,06%) | 1 (0,01%) | |
| Сультамициллин | J01CR04 | 4 | 0 (0,00%) | 4 (0,02%) | |
| Итого | 740 | 103 (6,13%) | 637 (3,69%) | ||
| Другие бета-лактамы |
Цефазолин | J01DB04 | 3 | 2 (0,1%) | 1 (0,01%) |
| Цефуроксим | J01DC02 | 10 | 9 (0,5%) | 1 (0,01%) | |
| Цефтриаксон | J01DD04 | 73 | 20 (1,2%) | 53 (0,3%) | |
| Цефиксим | J01DD08 | 68 | 4 (0,2%) | 64 (0,4%) | |
| Меропенем | J01DH02 | 1 | 1 (0,06%) | 0 (0,00%) | |
| Итого | 155 | 36 (2,14%) | 119 (0,69%) | ||
| Сульфаниламиды макролиды, линкозамиды |
Сульфаметоксазол+Триметоприм | J01EE01 | 8 | 5 (0,3%) | 3 (0,02%) |
| Эритромицин | J01FA01 | 2 | 1 (0,06%) | 1 (0,01%) | |
| Спирамицин | J01FA02 | 3 | 3 (0,2%) | 0 (0,00%) | |
| Джозамицин | J01FA07 | 21 | 3 (0,2%) | 18 (0,1%) | |
| Кларитромицин | J01FA09 | 169 | 7 (0,4%) | 162 (0,9%) | |
| Азитромицин | J01FA10 | 487 | 50 (3,0%) | 437 (2,5%) | |
| Линкомицин | J01FF02 | 1 | 1 (0,06%) | 0 (0,00%) | |
| Азитромицин, Кларитромицин |
J01FA10, J01FA09 |
1 | 0 (0,00%) | 1 (0,01%) | |
| Итого | 684 | 65 (3,87%) | 619 (3,59%) | ||
| Производные хинолона |
Офлоксацин | J01MA01 | 1 | 0 (0,00%) | 1 (0,01%) |
| Ципрофлоксацин | J01MA02 | 86 | 8 (0,5%) | 78 (0,5%) | |
| Норфлоксацин | J01MA06 | 1 | 0 (0,00%) | 1 (0,01%) | |
| Левофлоксацин | J01MA12 | 75 | 6 (0,4%) | 69 (0,4%) | |
| Моксифлоксацин | J01MA14 | 1 | 1 (0,06%) | 0 (0,00%) | |
| Гемифлоксацин | J01MA15 | 3 | 0 (0,00%) | 3 (0,02%) | |
| Итого | 167 | 15 (0,89%) | 152 (0,88%) | ||
| Другие АБ | Метронидазол | J01XD01 | 1 | 1 (0,06%) | 0 (0,00%) |
| Нитроксолин | J01XX07 | 1 | 0 (0,00%) | 1 (0,01%) | |
| Гидроксиметилхиноксалиндиоксид | J01XX | 3 | 0 (0,00%) | 3 (0,02%) | |
| Комбинации АБ разных групп |
Гидроксиметилхиноксалиндиоксид, Азитромицин |
J01XX, J01FA10 |
1 | 0 (0,00%) | 1 (0,01%) |
| Гидроксиметилхиноксалиндиоксид, Левофлоксацин |
J01XX, J01MA12 |
1 | 0 (0,00%) | 1 (0,01%) | |
| Азитромицин, Левофлоксацин |
J01FA10, J01MA12 |
1 | 0 (0,00%) | 1 (0,01%) | |
Включение препарата кагоцел в состав терапии ОРВИ и гриппа приводило к улучшению клинической картины заболевания, что выражалось в более существенном и опережающем группу сравнения регрессе всех анализируемых симптомов заболевания и, соответственно, скорейшем выздоровлении (рис. 4).
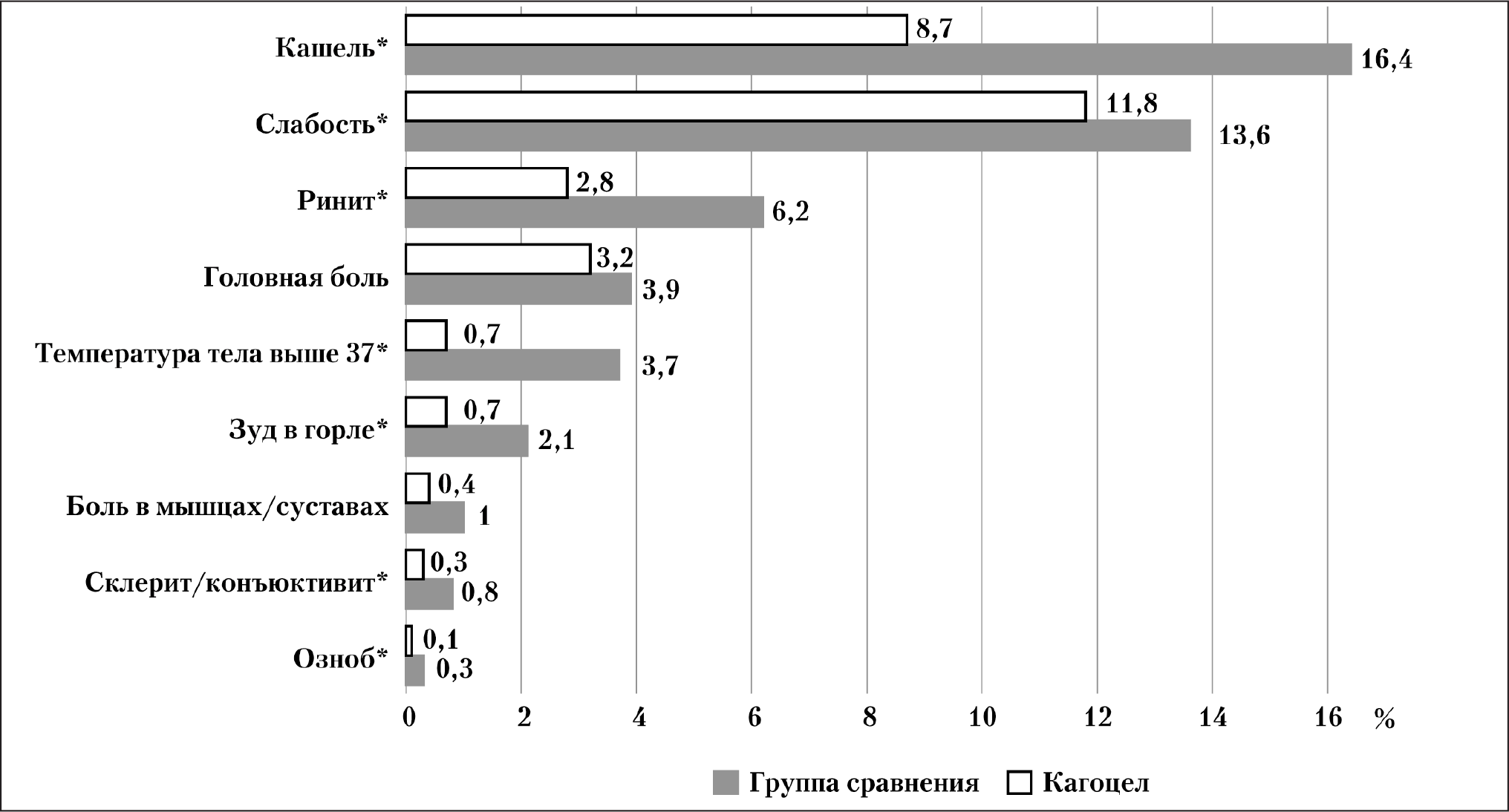
В группе сравнения полное купирование всех симптомов гриппа и ОРВИ зарегистрировано в 70,8% случаев, а в группе кагоцела — 77,9%, что в 1,10 раза больше (p<0,001). Выздоровление пациентов трудоспособного возраста наступало быстрее. Уже ко 2 визиту полное купирование всех симптомов ОРВИ и гриппа было зарегистрировано в 9,4% случаев: включая 5,5% пациентов группы сравнения и у 9,7% (в 1,76 раза больше) пациентов трудоспособного возраста, принимавших кагоцел. К 3 визиту остаточные явления были в 17,3 и 15,7% случаях соответственно. Неблагоприятный исход (определялся как неполное купирование всех симптомов заболевания) был установлен в 5,3% случаев, включая 11,6% пациентов группы сравнения и 4,8% (в 2,52 раза меньше) в группе кагоцела (p<0,001). Назначение кагоцела также способствовало улучшению исходов заболевания среди пациентов пенсионного возраста (p<0,05), однако частота неблагоприятного исхода у них была выше в 13,6% случаях в группе сравнения и в 8,4% случаях (в 1,62 раза реже) в группе препарата кагоцел (см. табл. 4).
| Возраст | Исход | Группа сравнения | Кагоцел | Всего |
|---|---|---|---|---|
| Трудоспособный (p<0,001) | Полное выздоровление к 2 визиту | 67 (5,5%) | 1348 (9,7%) | 1415 (9,4%) |
| Полное выздоровление к 3 визиту | 802 (65,6%) | 9670 (69,8%) | 10472 (69,4%) | |
| Наличие на 3-м визите 1-2 легких симптомов легкой степени | 211 (17,3%) | 2181 (15,7%) | 2392 (15,9%) | |
| Наличие на 3 визите 1-2 симптомов средней или тяжелой степени выраженности | 142 (11,6%) | 663 (4,8%) | 805 (5,3%) | |
| Пенсионный (р=0,047) | Полное выздоровление к 2 визиту | 19 (4,2%) | 171 (5,0%) | 190 (4,9%) |
| Полное выздоровление к 3 визиту | 300 (65,9%) | 2256 (66,3%) | 2556 (66,3%) | |
| Наличие на 3 м визите 1-2 симптомов легкой степени | 74 (16,3%) | 692 (20,3%) | 766 (19,9%) | |
| Наличие на 3 визите 1-2 симптома средней или тяжелой степени выраженности | 62 (13,6%) | 284 (8,4%) | 344 (8,9%) |
В среднем сроки выздоровления у пациентов группы кагоцел составили 7,23±1,75 суток от начала заболевания, в группе сравнения — 7,34±1,87 суток (p=0,070) при значимом сокращении сроков у фоново тяжелых больных в среднем на 1 день с 8 суток (7,84±1,81) до 7 дней (7,32±1,67) (p<0,01).
Обсуждение результатов
Системные антибиотики, назначение которых как правило связано с присоединением бактериальных осложнений ОРВИ и гриппа, были назначены врачами в условиях амбулаторного лечения в 9,3% случаях. При этом показания в виде осложнений, требующие назначения АБ, были зарегистрированы реже (8,3%), причем бактериальная пневмония диагностирована лишь в 0,7% случаев. Таким образом, несмотря на растущую резистентность к антибиотикам и доказанную нецелесообразность назначения АБ при острых респираторных вирусных инфекциях, подобная тактика продолжается, хотя и в не столь большом проценте. Это может отражаться на ухудшении исходов и увеличении сроков терапии ОРВИ и гриппа (а также сроков нетрудоспособности) на фоне необоснованного удорожания стоимости лечения. Полученные данные согласуются с мнением некоторых ученых, считающих необоснованность полипрагмазии в отношении антибиотикотерапии при респираторных вирусных инфекциях 11, 12. Наиболее часто назначаются АБ широкого спектра действия азитромицин и амоксициллин, что может быть связано с отсутствием проведения своевременного и адекватного микробиологического исследования.
Частота развития бактериальных осложнений и частота назначения антибиотиков для системного использования при ОРВИ и гриппе увеличивается пропорционально возрасту пациентов, наличия у них соматических заболеваний, тяжести настоящего вирусного заболевания, а также срокам начала лечения. Учитывая то, что отдаление сроков обращения за квалифицированной медицинской помощью прямо коррелирует с тяжестью 13, целесообразным является пропаганда раннего начала этиотропной патогенетически обоснованной противовирусной терапии.
Назначение противовирусного препарата кагоцел в составе комплексного симптоматического лечения ОРВИ и гриппа способствует значительному сокращению числа бактериальных осложнений в 1,65 раза, а также снижению назначений системной антибактериальной терапии в 1,51 раза, что приводит к улучшению исхода заболевания, ускорению регресса симптомов и сроков выздоровления. Следует подчеркнуть, что на фоне приема препарата кагоцел было зарегистрировано снижение частоты назначения таких АБ как пенициллины и различные бета-лактамы (в т.ч. амоксициллин, амоксициллин в сочетании с клавулановой кислотой, цефтриаксон). Значимая эффективность зарегистрирована при различных сроках начала терапии (1-е, 2-е и 3 сутки), что говорит о целесообразности применения кагоцела даже при запоздалом начале лечения. Важно отметить, что максимальная эффективность зарегистрирована у лиц трудоспособного возраста, что может быть связано с увеличением в группе пациентов пенсионного возраста больных с тяжелой соматической патологией.
Благодарности
Авторы статьи благодарят всех исследователей, принявших участие в наблюдательной программе «Лечение ОРВИ и гриппа в рутинной практике (FLU-EE)»: Айрумян С.А., Акопян С.Ш., Амбарцумян Л.С., Анисимова Н.В., Арвеладзе Ц., Архипова Н.М., Атоян Р.К., Афанасьева С.А., Бабуренкова Т.Д., Бадиул А., Бакалу В., Барбакадзе М., Басков В.Л., Бахшян К.А., Беглица Л., Бойко И.Н., Большакова Т.В., Борисевич Г.Г., Борисенко Ю.В., Бородина Т.К., Боярко Г.А., Брежнева С.В., Бушева С.Н., Вакула И.В., Васильева Т.В., Васина Е.М., Вахитова З.Р., Веденеева О.И., Векшина В.А., Виноградова Г.Н., Вишняков А.С., Воронюк Е., Вострухина М.Н., Вульфович И.В., Вязанкина Ю.В., Гарибян А., Гаспарян Р.Г., Геворгян Ж.К., Гейисова Е.В., Герр И.Е., Гилмуллина Ф.С., Гогаладзе Н., Голованова Е.Е., Голованова Н.В., Горелова М.С., Горкавцева О.Ю., Гребельская Т.П., Грекова Л.И., Григорьева И.Г., Григорян М.Н., Григорян Н.А., Григорян Н.С., Гридяева Л.Л., Гришина Е.В., Громацкий Е., Грушко В., Гукасян Н., Гульбина Е.Г., Гурьева Т.Н., Гусева И.Е., Давлетшина М.М., Давоян Т.З., Дарбинян С.В., Дашкевич О.В., Дгебуадзе Н., Девицына О.В., Дзадзамия Н., Добрынинский Д.А., Дюкова В.В., Егиазарян Р.С., Егорова С.В., Ежова Г.Ю., Елисеенко Л.Ф., Жезлова Г.А., Жмуровская Т.Д., Завидей К., Завозина Л.А., Загребнева Н.И., Заерова Л.М., Закарян С.С., Закирова А.М., Залялов М.А., Замятина Л.Л., Захарова И.Г., Захарова О.С., Зограбян Д.А., Зонова С.В., Игнатьева А.Л., Идрисов И.Р., Идрисова З.Д., Илуридзе Н., Ильин А.А., Ишимбаев И.Р., Ишимбаева А.Х., Карагезян Л.В., Карапетян А.В., Карапетян Л.С., Карапетян М.Г., Квернадзе М., Кейдер Е.В., Киприянова Е.В., Кириллова М.Н., Киронда О., Киселева Е.В., Клокова Т.А., Ковалева Л.Н., Кожухова Е., Козарь Е., Колосовская А.А., Копысова Г.Н., Коробицына О.А., Костарев О.В., Котикова Г.А., Круглова Н.В., Крячко Е.Г., Кспоян С.Т., Кудрякова Н.А., Кудряшова Н.О., Кузнецова С.М., Кузьмина Н.И., Кулимбетова Л.А., Кутян Т.А., Кушникова А.Р., Ларина В.К., Левова О.Н., Левченко Г.И., Ломжева Л.М., Лукина Н.Ф., Лунгу Л., Львова С.М., Малыхина В.А., Малышева А., Маннанова А.Н., Манукян А.К., Маринюк И., Марченко Е.А., Махсудян Н.А., Меликян В.С., Меньшикова Г.Н., Михайленко А.В., Мкртчян Н.Ю., Можина Л.Н., Мозина Л.В., Мусатова Л.А., Мындряну Ю., Назарова Т.А., Накудашвили Е., Насртдинов Р.Р., Настас И., Нахапетян М.М., Никулина И.В., Новак В., Новак Л., Нургалеева Л.А., Оганисян Н.Р., Одинцова Т.А., Озерчук А.А., Озерчук Г.Ф., Орехова Е.Э., Орлова В.Ф., Осинцева О.В., Осипова Е.В., Панфилова И.Ю., Панфилова Л.А., Папоян Ж., Парахина В.В., Печерская М.Н., Пирцхелаури Е., Пистун О., Плачинта Н., Позднякова О.Ю., Полторацкая Е.В., Полякова Л.Г., Попова О.А., Прокудина И.А., Прыгунова Т.С., Пустынская М.С., Раменская Т.Е., Распопов А.С., Рубенкова А.А., Руснак А., Руснак О., Рыбицкая Т.С., Рязанова Н.В., Саакян Л.Б., Савельева О.В., Савинкина Н.В., Семовских Н.А., Серикова С.П., Серобян С.С., Серякова И.В., Сикорская Л., Симонова А.В., Ситников И.Г., Слесарева Д.С., Смирнова В.В., Смоль Д., Соколова Е.И., Сокорова Г.А., Сорокина Э.А., Соселия И., Софин А.Б., Стефанко О.М., Стульникова О.В., Сырбу В., Таболина Е.Е., Тадевосян Л.К., Татаренко Е.М., Ташник Л., Тернавский С.Н., Тетерина И.А., Тимофеева Л.Н., Тимошенко А.И., Тимошенко Е.В., Тишенко Е., Токарева К.А., Топчий Е.Е., Тороян Г.А., Тростина С., Угарова Е.А., Урвант О.В., Уткина О.В., Уткина И.И., Ушатый А.А., Федотова Н.В., Федотова О.П., Филипенко С.С., Хартукова С.Ю., Харченко О.А., Хачатрян С.Ю., Хведынич А.С., Хотеенкова Н.В., Храброва С.Л., Царева Т.В., Черневская Т., Чернышева М.В., Шакирова В.Г., Шмидько С.В., Шуликина О.В., Яким Л.
Литература/References
- Львов Н.И., Лихопоенко В.П. Острые респираторные заболевания. Руководство по инфекционным болезням: 4-е изд., доп. и перер. СПб.: Фолиант; 2011, 2: III: 7—122. / L'vov N.I., Lihopoenko V.P. Ostrye respiratornye zabolevanija. Rukovodstvo po infekcionnym boleznjam: 4-e izd., dop. i perer. SPb.: Foliant; 2011, 2: III: 7—122. [in Russian]
- Романова И.В., Суздальцев А.А. Грипп. Самара: ООО «Издательство Ас Гард»; 2013. / Romanova I.V., Suzdal'cev A.A. Gripp. Samara: OOO «Izdatel'stvo As Gard»; 2013. [in Russian]
- Еропкин М.Ю., Карпова Л.С., Коновалова Н.И., Лобова Т.Г., Петрова П.А., Щеканова С.М. Грипп в сезоне 2014—2015 гг. в России: эпидемиология и свойства вирусов. Эпидемиол инфекц бол 2015; 20: 6: 4—11. / Eropkin M.Ju., Karpova L.S., Konovalova N.I., Lobova T.G., Petrova P.A., Shhekanova S.M. Gripp v sezone 2014-2015 gg. v Rossii: jepidemiologija i svojstva virusov. Jepidemiol infekc bol 2015; 20: 6: 4—11. [in Russian]
- Государственный доклад «О санитарно-эпидемиологической обстановке в Российской Федерации в 2010 году». М.: ФГУ Центр гигиены и эпидемиологии; 2011. / Gosudarstvennyj doklad «O sanitarnojepidemiologicheskoj obstanovke v Rossijskoj Federacii v 2010 godu». M.: FGU Centr gigieny i jepidemiologii; 2011. [in Russian]
- Львов Д.К., Бурцева Е. И., Колобухина Л.В., Федякина И.Т., Кириллова Е.С., Трушакова С.В. и др. Вирусологические, эпидемиологические, клинические, молекулярно-генетические особенности эпидемии гриппа 2015—2016 гг: доминирование вируса гриппа А (H1N1) pdm09 в России и странах северного полушария. Вопр вирусол 2016: 61: 4: 159—166. / L'vov D.K., Burceva E. I., Kolobuhina L.V., Fedjakina I.T., Kirillova E.S., Trushakova S.V. i dr. Virusologicheskie, jepidemiologicheskie, klinicheskie, molekuljarno-geneticheskie osobennosti jepidemii grippa 2015—2016 gg: dominirovanie virusa grippa A (H1N1) pdm09 v Rossii i stranah severnogo polusharija. Vopr virusol 2016: 61: 4: 159—166. [in Russian]
- Казюкова Т.В., Радциг Е.Ю., Панкратов И.В., Алеев А.С. Сравнительная оценка эффективности двух противовирусных препаратов в лечении гриппа и ОРВИ у детей 6—12 лет. Педиатрия 2015; 6: 105—112. / Kazjukova T.V., Radcig E.Ju., Pankratov I.V., Aleev A.S. Sravnitel'naja ocenka jeffektivnosti dvuh protivovirusnyh preparatov v lechenii grippa i ORVI u detej 6—12 let. Pediatrija 2015; 6: 105—112. [in Russian]
- Кокорева С.П., Сахарова Л.А., Куприна Н.П. Этиологическая характеристика и осложнения острых респираторных инфекций у детей. Вопр современ педиатр 2008; 7: 1: 47—50. / Kokoreva S.P., Saharova L.A., Kuprina N.P. Jetiologicheskaja harakteristika i oslozhnenija ostryh respiratornyh infekcij u detej. Vopr sovremen pediatr 2008; 7: 1: 47—50.
- Скворцов В.В., Тумаренко А.В., Скворцова Е.М. Актуальные вопросы диагностики и лечения гриппа. Поликлиника, инфекц бол 2012; 2: 104—107. / Skvorcov V.V., Tumarenko A.V., Skvorcova E.M. Aktual'nye voprosy diagnostiki i lechenija grippa. Poliklinika, infekc bol 2012; 2: 104—107. [in Russian]
- Купченко А.Н., Понежева Ж.Б. Современные принципы диагностики и лечения ОРВИ. Архив внутр мед 2016; 27: 1: 6—12. / Kupchenko A.N., Ponezheva Zh.B. Sovremennye principy diagnostiki i lechenija ORVI. Arhiv vnutr med 2016; 27: 1: 6—12.
- Романцов М.А. Респираторные заболевания у часто болеющих детей. М.: Гэотар Медиа; 2014. / Romancov M.A. Respiratornye zabolevanija u chasto bolejushhih detej. M.: Gjeotar Media; 2014. [in Russian]
- Нисевич Л.Л., Волков К.С., Алексеева А.А., Томилова А.Ю., Баранник В.А., Эфендиева К.Е. Подходы к терапии острых респираторных инфекций и гриппа при сезонном увеличении заболеваемости. Вопр современ педиатр 2015; 14: 1: 64—69. / Nisevich L.L., Volkov K.S., Alekseeva A.A., Tomilova A.Ju., Barannik V.A., Jefendieva K.E. Podhody k terapii ostryh respiratornyh infekcij i grippa pri sezonnom uvelichenii zabolevaemosti. Vopr sovremen pediatr 2015; 14: 1: 64—69. [in Russian]
- Таточенко В.К. Антибиотико- и химиотерапия инфекций. М.: Континент-Пресс; 2008. / Tatochenko V.K. Antibiotiko- i himioterapija infekcij. M.: Kontinent-Press; 2008. [in Russian]
- Фазылов В.Х., Ситников И.Г., Силина Е.В., Шевченко С.Б., Можина Л.Н., Замятина Л.Л. и др. Лечение больных ОРВИ и гриппом в повседневной клинической практике (результаты многоцентрового международного наблюдательного исследования FLU-EE). Тер архив 2016; 11: 61—68. / Fazylov V.H., Sitnikov I.G., Silina E.V., Shevchenko S.B., Mozhina L.N., Zamjatina L.L. i dr. Lechenie bol'nyh ORVI i grippom v povsednevnoj klinicheskoj praktike (rezul'taty mnogocentrovogo mezhdunarodnogo nabljudatel'nogo issledovanija FLU-EE). Ter arhiv 2016; 11: 61—68. [in Russian]
